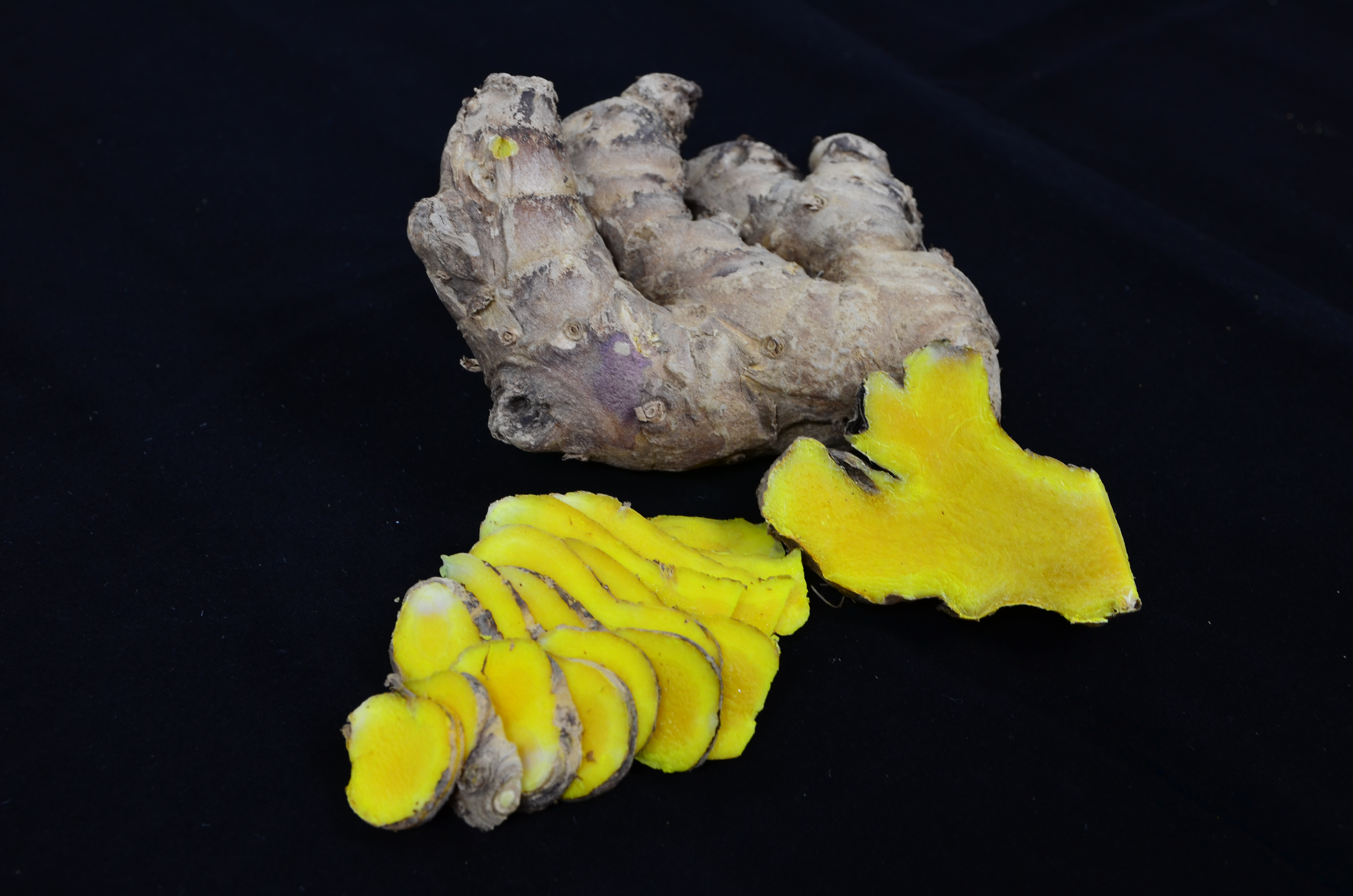
ไพล
- ชื่อ
- ส่วนของพืชที่ใช้
- การกระจายตัวทางภูมิศาสตร์/แหล่งที่มา
- ลักษณะทางพฤกษศาสตร์
- การเพาะปลูก
- สรรพคุณและการใช้สมุนไพรพื้นฐานตามภูมิปัญญาไทยด้านเครื่องสำอาง
- สารเคมีที่เป็นองค์ประกอบ
- สารออกฤทธิ์ หรือ สารสำคัญ
ชื่อวิทยาศาสตร์
Zingiber montanum (J.Koenig) Link ex A. Dietr.
ชื่อวงค์
ZINGIBERACEAE
ชื่อสมุนไพร
ไพล
ชื่ออังกฤษ
Zingiber montanum
ชื่อพ้อง
Amomum cassumunar (Roxb.) Donn
Amomum montanum J.Koenig
Amomum xanthorhiza Roxb. exSteud.
Cassumunar roxburghii Colla
Jaegera montana (J.Koenig) Giseke
Zingiber anthorrhiza Horan.
Zingiber cassumunar Roxb.
Zingiber cassumunar var. palamauense Haines
Zingiber cassumunar var. subglabrum Thwaites
Zingiber cliffordiae Andrews
Zingiber luridum Salisb.
Zingiber montanum (J. König ex Retz.) Theilade
Zingiber purpureum Roscoe
Zingiber purpureum var. palamauense (Haines) K.K.Khanna
Zingiber xantorrhizon Steud.
ชื่อท้องถิ่น
ปูลอย, ปูเลย, มิ้นสะล่าง, ว่านไฟ
ชื่อ INCI
-
ส่วนของพืชที่ใช้
การกระจายตัวทางภูมิศาสตร์/แหล่งที่มา
พบกระจายไปทั่วบริเวณเขตร้อนของเอเชียและเอเชียตะวันออกเฉียงใต้ (4) พบได้ในป่าบริเวณที่มีดินค่อนข้างสมบูรณ์มีสารอินทรีย์ พื้นที่ร่มรำไรไปถึงพื้นที่โล่งแจ้งตามชายป่า บริเวณที่ค่อนข้างแห้งในป่าโปร่ง ป่าเบญจพรรณในระดับพื้นล่างถึงป่าดิบเขาสูง (5)
ลักษณะทางพฤกษศาสตร์
ไม้ล้มลุก สูง 0.7 - 1.5 ม. มีเหง้าใต้ดิน เปลือกนอกสีน้ำตาลแกมสีเหลือง เนื้อในสีเหลืองแกมสีเขียว มีกลิ่นเฉพาะ แทงหน่อหรือลำต้นเทียมขึ้นเป็นกอ ใบเดี่ยวเรียงสลับ รูปขอบขนานแกมรูปใบหอก กว้าง 3.5 - 5.5 ซม. ยาว 18 - 35 ซม. ช่อดอก เจริญจากเหง้าใต้ดิน กลีบดอกสีเหลืองอ่อนหรือสีนวล ใบประดับสีม่วงเข้มขอบสีเขียว ผลเป็นผลแห้ง รูปกลม (3)
การเพาะปลูก
พื้นที่เหมาะสมในการปลูกในประเทศไทย
พื้นที่ดอนน้ำไม่ท่วมขังพื้นที่สวนผักพื้นที่ปลูกพืชไร่ทั่วไปหัวไร่ปลายนา ทั่วทุกภาคของประเทศไทยทุกจังหวัดของประเทศไทย
การคัดเลือกพันธุ์ (พันธุ์ที่นิยมปลูกในประเทศไทย)
พันธุ์ที่ใช้เป็นยา: พันธุ์พื้นบ้านทั่วไป
พันธุ์ที่ใช้เป็นอาหาร: ในประเทศไทย ไม่ใช้ไพลทำเป็นอาหาร
การขยายพันธุ์
ขยายพันธุ์ด้วยการใช้เหง้าเมื่อขุดไพลในฤดูเก็บเกี่ยวแล้วเก็บเหง้าไพลเอาไว้ทำพันธุ์โดยขุดมาไม่ต้องล้างน้ำ เก็บผึ่งไว้ในร่มอย่าให้โดนน้ำเพื่อเอาไว้ทำพันธุ์
การปลูก/สภาพแวดล้อมที่เหมาะสมในการปลูก
ฤดูกาลเพาะปลูกนิยมปลูกในช่วงเดือนพฤษภาคม – กรกฎาคมซึ่งเป็นช่วงฤดูฝน
การเตรียมดินโดยการไถดะไถแปรและไถพรวนยกร่องกว้างประมาณ 1 ม. เว้นทางเดินเป็นร่อง
ประมาณ 50 ซม. หว่านปุ๋ยคอกหรือปุ๋ยหมักบนแปลงปลูก
วิธีการปลูก นำเหง้าไพลฝังลงบนแปลงหลุมห่างกัน 30 ซม. ระยะแถว 30 ซม. กลบดินให้มิดเหง้าไพล รดน้ำให้ชุ่มอยู่เสมอ ประมาณ 3 - 4 สัปดาห์ ไพลจะงอกขึ้นมาเป็นต้นใหม่
การปฏิบัติดูแลรักษา
การให้ปุ๋ยเมื่อไพลได้ 1 - 2 เดือนนำการพรวนดินและใส่ปุ๋ยด้วยปุ๋ยวิทยาศาสตร์ 16-16-16 ตลอดอายุควรให้ปุ๋ยประมาณ 1 - 2 ครั้ง
การให้น้ำถ้าปลูกฤดูฝนปล่อยตามธรรมชาติได้
การกำจัดวัชพืชควรกำจัดวัชพืชพร้อมกับการพรวนดินและใส่ปุ๋ย
การป้องกันกำจัดโรคและแมลงศัตรูการป้องกันโรคและแมลงควรใช้สารจำพวกสารสะเดาและสารชีวภาพ (ไม่ควรใช่สารเคมีจะสะสมในเหง้า)
การเก็บเกี่ยวและการปฏิบัติหลังเก็บเกี่ยว
ฤดูกาลการเก็บเกี่ยวไพลจะเก็บเกี่ยวในฤดูแล้งช่วงเดือนธันวาคม - เมษายนโดยจะเก็บเกี่ยวเมื่ออายุ 1 - 2 ปีขึ้นไป
วิธีการเก็บเกี่ยวเก็บเกี่ยวโดยการขุดพอไพลแก่ต้นจะเริ่มยุบและเหลือง เริ่มขุดโดยใช้แรงงานคนให้ขุดด้วยเสียมหรือจอบ ระวังอย่าใหเหง้าเสียหายแล้วสลัดดินออกส่งแปรรูปหรือจำหน่ายต่อไป
การแปรรูปหลังการเก็บเกี่ยวเมื่อได้เหง้าไพลมาแล้วล้างน้ำให้สะอาด หั่นบางๆแล้วตากแดดทันที ประมาณ 4 - 5 วันจนแห้งแล้วนำไปอบอีกครั้งจนแห้งสนิท
การบรรจุและการเก็บรักษาเมื่อได้ไพลแห้งมาแล้วใส่กระสอบเพื่อส่งจำหน่ายต่อไปหรือถ้าจะเก็บใส่กระสอบโปร่งๆหรือถุงปุ๋ยสะอาดโดยเก็บไว้ในห้องที่มีีอุณหภูมิปกติ
การจำหน่าย
เหง้าไพลสด ราคากิโลกรัมละ 15-50 บาท
เหง้าไพลแห้ง ราคากิโลกรัมละ 100-150 บาท
(27)
สรรพคุณและการใช้สมุนไพรพื้นฐานตามภูมิปัญญาไทยด้านเครื่องสำอาง
เหง้า ช่วยสมานแผล (3)
สารเคมีที่เป็นองค์ประกอบ
สารกลุ่มฟีนิลบิวทานอยด์ (phenylbutanoids) ได้แก่
(E)-1-(3,4-dimethoxyphenyl)butadiene (DMPBD),
(E)-4-(3,4-dimethoxyphenyl)but-3-en-1-ol (Compound D),
(E)-4-(3,4-dimethoxyphenyl)but-3-en-1-yl acetate,
4-(2,4,5-trimethoxyphenyl)but-1-3-diene,
(±)-trans-3-(4-hydroxy-3-methoxyphenyl)-4-[(E)-3,4-dimethoxystyryl]cyclohex-1-ene,
(±)-trans-3-(3,4-dimethoxyphenyl)-4-[(E )-3,4-dimethoxy-styryl]cyclohex-1-ene,
phlains I, phlains II, phlains III, phlains IV, phlains V และphlains VI (7 - 17)
สารกลุ่มเคอร์คิวมินอยด์ (curcuminoids) ได้แก่ curcumin,cassumunins A, B และ C, cassumunarins A, B และ C (12-13, 17 - 19)
สารกลุ่มสารประกอบแอลดีไฮด์ (aldehyde compound) ได้แก่ 2,4,5-trimethoxybenzaldehyde (asaraldehyde) (17)
สารกลุ่มเซสควิเทอร์ปินอยด์ (sesquiterpenoids) ได้แก่ zerumbone (12)
สารกลุ่มอนุพันธ์ของสารเคมเฟอรอล (kaempferol derivatives) ได้แก่ kaempferol 3-O-methyl ether, kaempferol 3-O-α-rhamnopyranoside, kaempferol 3-O-α-(4′′-O-acetyl)rhamnopyranoside, kaempferol 3-O-α-(3′′-O-acetyl)rhamnopyranosideและ kaempferol 3-O-α-(3′′,4′′-di-O-acetyl)rhamnopyranoside (12)
สารกลุ่มน้ำมันหอมระเหย (essential oil) ได้แก่ α-thujene, α-pinene, camphene, sabinene, β-pinene, myrcene, α-phellandrene, α-terpinene, p-cymene, limonene, β-phellandrene, 1,8-cineole, (E)-β-ocimene, ɣ-terpinene, terpinolene, linalool, borneol, terpinen-4-ol, α-terpineol, α-terpinyl acetate, ar-curcumene, α-zingiberene, α-muurolene, β-bisabolene, β-curcumene, myristicin, β-sesquiphellandrene, humulene epoxide II และ caryophyllene oxide (16)
สารกลุ่มฟีนิลบิวทานอยด์ (phenylbutanoids)
สารกลุ่มเคอร์คิวมินอยด์ (curcuminoids)
สารกลุ่มสารประกอบแอลดีไฮด์ (aldehyde compound)
สารกลุ่มเซสควิเทอร์ปินอยด์ (sesquiterpenoids)
สารกลุ่มอนุพันธ์ของสารเคมเฟอรอล (kaempferol derivatives)
สารกลุ่มน้ำมันหอมระเหย (essential oil)
สารออกฤทธิ์ หรือ สารสำคัญ
- สารออกฤทธิ์ต้านอักเสบ ได้แก่ สารกลุ่มฟีนิลบิวทานอยด์ เช่นDMPBD (7), เคอร์คิวมินอยด์เช่น cassumunarins A, B และ C (18)
- สารออกฤทธิ์ต้านอนุมูลอิสระ ได้แก่ สารกลุ่มเคอร์คิวมินอยด์เช่น cassumunarins A, B และ C (18), cassumunins A, B และ C และ curcumin (19)
แนวทางการควบคุมคุณภาพ (วิเคราะห์ปริมาณสารสำคัญ)
วิธีตรวจสอบ / การแยกสกัดและพิสูจน์เอกลักษณ์ (20)
- นำผงไพลมา 500 มก. เติมคลอโรฟอร์ม 5 มล. ตั้งทิ้งไว้ 5 นาที แล้วกรอง ได้สารละลาย (solution 1)นำสารละลาย 1 มล. สังเกตใต้แสงอัลตร้าไวโอเลตความยาวคลื่น 366 นาโนเมตร พบสารละลายเรืองแสงสีเขียวเหลือง
- นำสารละลาย1 มล. เติม acetic anhydride-sulfuric acid 0.2 มล. สังเกตสารละลายเปลี่ยนเป็นสีน้ำตาลแดง
- นำสารละลาย 1 มล. เติม boric acid-methanol 1 มล. สังเกตสารละลายเปลี่ยนเป็นสีส้ม
- วิเคราะห์ด้วยเทคนิค ทีแอลซี หรือ วิธีโครมาโตกราฟีแบบชั้นบาง (Thin-Layer Chromatography, TLC) โดยมีวัฏภาคคงที่เป็น silica gel GF254 และวัฏภาคเคลื่อนที่เป็น hexane : ethyl acetate (70:30) แล้วตรวจสอบด้วยน้ำยาพ่น anisaldehyde และ vanillin/sulfuric acid (20)
ข้อกำหนดคุณภาพตามเภสัชตำรับ
Thai Herbal Pharmacopoeia (THP) (20) ได้มีการกำหนดมาตรฐานของเหง้าไพลดังนี้
ปริมาณความชื้น (%w/w) ไม่เกิน 13.0
ปริมาณสิ่งแปลกปลอม (%w/w) ไม่เกิน 2.0
ปริมาณเถ้าที่ไม่ละลายในกรด (%w/w) ไม่เกิน 3.0
ปริมาณเถ้ารวม (%w/w) ไม่เกิน 9.0
ปริมาณสารสกัดด้วยเฮกเซน (%w/w) ไม่น้อยกว่า 3.0
ปริมาณสารสกัดด้วยคลอโรฟอร์ม (%w/w) ไม่น้อยกว่า 5.0
ปริมาณน้ำมันหอมระเหย (%w/w) ไม่น้อยกว่า 2.0
การวิเคราะห์สารกลุ่ม phenylbutanoids
การวิเคราะห์ด้วย reversed - phase HPLC มีตัวอย่างการศึกษาดังนี้ (15)
Stationary Phase: TSK-gel ODS-80 Tm
Mobile phase:
2% acetic acid :methanol อัตราส่วน 52:48 (ที่ 0 - 20 นาที)
2% acetic acid :methanol อัตราส่วน 50:50 (ที่ 22 - 38 นาที)
2% acetic acid :methanol อัตราส่วน 52:48 (ที่ 40 - 60 นาที)
Detection: ตรวจสอบที่ความยาวคลื่น 254 nm
การวิเคราะห์สารกลุ่มน้ำมันหอมระเหย
การวิเคราะห์ด้วย gas chromatography interfaced to a mass spectrometer (GC-MS) มีตัวอย่างการศึกษาดังนี้ (11)
วิเคราะห์หาองค์ประกอบทางเคมีของน้ำมันหอมระเหยด้วยเครื่อง Shimadzu QP5050A gas chromatography interfaced to a mass spectrometer (GC-MS)
Column: column DB5 (60 cm × 0.25 mm i.d., composed of 5% phenylmethylpolysiloxane)
Injection volume: 1 µl (in C5H12)
Injector temperature: 250 °C
Detector temperature: 250 °C
Oven temperature : เริ่มต้น ที่ 60°C เป็นเวลา 3 นาที และเพิ่มอุณหภูมิ 1 °C/นาทีจนถึง 80 °C และคงที่เป็นเวลา 3 นาที และเพิ่มอุณหภูมิ 3 °C/นาทีจนถึง 120 °C และคงที่เป็นเวลา 3 นาทีและเพิ่มอุณหภูมิ 4 °C/นาทีจนถึง 240 °C และคงที่เป็นเวลา 3 นาที
ตรวจพิสูจน์องค์ประกอบทางเคมีของน้ำมันหอมระเหยไพลโดยการเปรียบเทียบmass spectral ของสารที่ได้กับค่าของ National Institute of Standards and Technology Mass Spectral database (NIST-MS)
การศึกษาทางคลินิก
การศึกษาเกี่ยวกับผิวหน้า
ฤทธิ์ต้านสิว (F006)
การศึกษาทางคลินิกเพื่อทดสอบประสิทธิผลและความปลอดภัยในการรักษาสิวระดับรุนแรงเล็กน้อยถึงปานกลางของผลิตภัณฑ์เจลที่ทําจากน้ำมันไพลปริมาณ 1% (ไม่ระบุแหล่งที่มาและวิธีการเตรียมสารสกัด) โดยเปรียบเทียบกับยาหลอก ในอาสาสมัครสุขภาพดี เพศชาย จำนวน 60 ราย เพศชายอายุระหว่าง 18-25 ปี เป็นสิวชนิดacne vulgaris ซึ่งมีความรุนแรงเล็กน้อยถึงปานกลางและไม่มีสิวอักเสบชนิด nodule, cyst หรือ sinus tract กล่าวคือมีสิวไม่อักเสบน้อยกว่า 20 จุดและมีสิวอักเสบน้อยกว่า 50 จุดรูปแบบการศึกษาเป็น randomized, double blinded, placebo controlled trial ให้อาสาสมัครล้างหน้าวันละ 2ครั้งตอนเช้าและเย็นด้วยผลิตภัณฑ์ล้างหน้าที่อาสาสมัครใช้เป็นประจําหลังจากเช็ดหน้าให้แห้งจึงแต้มสิวโดยทารอบ ๆ บริเวณที่เป็นสิวและบริเวณที่มักจะเป็นสิวด้วยเจลไพลความเข้มข้น 1% หรือยาหลอกบันทึกการใช้ผลิตภัณฑ์ ลงในสมุดบันทึกประจําตัวประเมินผลการทดสอบ โดยมีตัวชี้วัดหลักคือ ร้อยละการลดลงของจำนวนสิว ทำการประเมินผล ณ สัปดาห์ที่ 2, 4 และ 8 ผลการศึกษาพบว่าอาสาสมัครกลุ่มที่ได้รับเจลไพลมีร้อยละการลดลงของจำนวนสิวทั้งหมด (สิวชนิดอักเสบและไม่อักเสบ) สูงกว่ากลุ่มที่ได้รับยาหลอก ณ สัปดาห์ที่ 2 และ 4 ตามลำดับ เท่ากับ 6 และ 12 และมีร้อยละของการลดลงของจํานวนสิวชนิดไม่อักเสบ สูงกว่ากลุ่มที่ได้รับยาหลอกเท่ากับ 14 และ 26 ณสัปดาห์ที่2และ4 ตามลําดับ อย่างไรก็ตามความแตกต่างดังกล่าวไม่มีนัยสําคัญทางสถิติและสัปดาห์ที่ 8 พบว่าร้อยละของการลดลงของจํานวนสิวไมแตกต่างกันระหวางเจลไพลและยาหลอกจํานวนสิวไมีอักเสบในกลุ่มที่ได้รับเจลไพลลดลงอย่างมีนัยสําคัญทางสถิติ ในสัปดาห์ที่ 2 และ4 เมื่อเปรียบเทียบกับจุดเริ่มต้นในขณะที่สิวไม่อักเสบในกลุ่มที่ได้รับยาหลอกลดลงอย่างไม่มีนัยสําคัญทางสถิติ เมื่อเปรียบเทียบกับจุดเริ่มต้นค่าเฉลี่ยร้อยละการลดลงของสิวอักเสบที่สัปดาห์ที่ 2 และ 4 ในกลุ่มที่ได้เจลไพลมีค่าน้อยกว่ากลุ่มที่ได้รับยาหลอกแต่ไม่มีนัยสําคัญทางสถิติร้อยละความสําเร็จของการรักษาที่สัปดาห์ที่ 8 ของกลุ่มที่ได้รับเจลไพลเท่ากับร้อยละ39และกลุ่มที่ได้รับยาหลอกเท่ากับร้อยละ31ซึ่งแตกต่างอย่างไม่มีนัยสําคัญทางสถิติการใช้จลไพลมีความปลอดภัยและไมพบรายงานอาการข้างเคียงความร่วมมือในการใชผลิตภัณฑ์มีมากกว่าร้อยละ90โดยสรุปเจลไพลมีแนวโน้มให้ผลการรักษาสิวเล็กน้อยถึงปานกลางโดยสามารถเห็นผลการรักษาไดภายในเดือนแรกเมื่อเทียบกับยาหลอก (6)
การศึกษาฤทธิ์ทางเภสัชวิทยา
การศึกษาเกี่ยวกับผิวกาย
ฤทธิ์ทำให้ผิวขาว (S001)
การศึกษาฤทธิ์ยับยั้งการทำงานของเอนไซม์ไทโรซิเนส (% tyrosinase inhibition) ของพืชสมุนไพรไทย 18 ชนิดโดยคัดเลือกสมุนไพรจากจังหวัดเชียงใหม่ ตัวอย่างสมุนไพรได้มีการพิสูจน์ความถูกต้องและเก็บตัวอย่างพรรณไม้อ้างอิงงานวิจัย (voucher specimen) โดยหอพรรณไม้ คณะเภสัชศาสตร์ มหาวิทยาลัยเชียงใหม่สกัดน้ำมันหอมระเหยด้วย Clevenger-type apparatus ทดสอบฤทธิ์ยับยั้งการทำงานของเอนไซม์ไทโรซิเนสโดยวิธีmodified dopachrome methodผลการทดสอบพบว่าน้ำมันหอมระเหยจากเหง้าไพลมีฤทธิ์ในการยับยั้งการทำงานของเอนไซม์ไทโรซิเนส มีค่า % tyrosinase inhibition >30% (21)
ฤทธิ์ต้านสิว (S005)
การศึกษาฤทธิ์ของน้ำมันหอมระเหยสมุนไพร (22) ชนิดจากบริษัทอุตสาหกรรมเครื่องหอมไทย-จีนจำกัด (Thai China Flavors & Fragrances Industry Co. Ltd) ในการยับยั้งเชื้อแบคทีเรียสาเหตุของการเกิดสิว Propionibacterium acnes (P. acnes) 5 strains ได้แก่ DMST No. 14916, 14917, 14918, 21823 และ 21824 ด้วยวิธี disc diffusion พบว่าน้ำมันหอมระเหยจากเหง้าไพลมีฤทธิ์ยับยั้ง P. acnes DMST No. 14916, 14917, 14918, 21823 และ 21824 ให้ค่า inhibition zone เท่ากับ 13.5 ± 2.0, 13.9 ± 0.9, 14.7 ± 1.7, 13.3 ± 0.7 และ 15.7 ± 2.2 มม. ตามลำดับ ในขณะที่ tetracycline 30ไมโครกรัม/disc มีฤทธิ์ยับยั้ง P. acnes DMST No. 14916, 14917, 14918, 21823 และ 21824 ให้ค่า inhibition zone เท่ากับ35.5 ± 4.6, 35.3 ± 3.1, 35.5 ± 3.8, 35.3 ± 3.0 และ 35.8 ± 2.8, erythromycin 15ไมโครกรัม/disc มีฤทธิ์ยับยั้ง P. acnes DMST No. 14916, 14917, 14918, 21823 และ 21824 ให้ค่า inhibition zone เท่ากับ30.9 ± 1.4, 31.3 ± 2.8, 29.1 ± 1.3, 29.2 ± 1.1 และ 28.6 ± 1.5 และ clindamycin 2 ไมโครกรัม/disc มีฤทธิ์ยับยั้งP. acnes DMST No. 14916, 14917, 14918, 21823 และ 21824 ให้ค่าinhibition zone เท่ากับ 31.0 ± 1.3, 31.2 ± 1.5, 30.4 ± 1.6, 29.4 ± 0.8 และ 29.1 ± 1.7 ตามลำดับ และการทดสอบด้วยวิธี agar dilutionให้ค่าความเข้มข้นต่ำสุดที่มีผลยับยั้งการเจริญของเชื้อ (minimum inhibitory concentrations; MIC) ต่อเชื้อ P. acnesทุก strains เท่ากับ4 % v/v (22))
การศึกษาฤทธิ์ต้านแบคทีเรียสาเหตุของการเกิดสิว P. acnes, Staphylococcus aureus และ S. epidermidis ของน้ำมันหอมระเหยจากเหง้าไพลจากบริษัทอุตสาหกรรมเครื่องหอมไทย-จีนจำกัด และเจลที่ทําจากน้ำมันหอมระเหยจากเหง้าไพล 5% ในหลอดทดลอง ด้วยวิธี broth dilution พบว่าน้ำมันหอมระเหยจากเหง้าไพลมีค่าความเข้มข้นต่ำสุดที่มีผลในการฆ่าเชื้อ (minimum bactericidal concentration; MBC) เท่ากับร้อยละ 0.62 โดยปริมาตร เปรียบเทียบกับ tea tree oil มีค่า MBC เท่ากับร้อยละ 0.5 โดยปริมาตร ส่วนค่า MBC ต่อเชื้อ S. epidermidis ATCC 12228 เท่ากับร้อยละ 2.5 โดยปริมาตร เปรียบเทียบกับยา ampicillin มีค่า MBC เท่ากับ 0.24 มคก./มล. สำหรับน้ำมันหอมระเหยจากเหง้าไพลในรูปแบบเจล 5% พบว่ามีค่า MBC ต่อเชื้อ S. aureus และS. epidermidisเท่ากับ 79มก./มล. และ 78.5 มก./มล. เปรียบเทียบกับยา Garamycin® cream (ประกอบด้วย gentamicin sulfate 1 มก./ก.) มีค่า MBC ต่อเชื้อ S. aureusและS. epidermidis เท่ากับ2.3 มก./มล.และ 2.2 มก./มล.ตามลำดับ (23)
ฤทธิ์ต้านอนุมูลอิสระ (S006)
การศึกษาฤทธิ์ต้านอนุมูลอิสระของผงเหง้าไพลแห้งจากกรุงเทพมหานคร สกัดด้วยตัวทำละลายเอทานอลและเฮกเซน ด้วยเทคนิค supercritical CO2 fluidทดสอบฤทธิ์ต้านอนุมูลอิสระในเซลล์มะเร็งตับของมนุษย์ชนิด HepG2 (human hepatoma cell line) และเซลล์แมคโครฟาจชนิด RAW 264.7 ที่ถูกเหนี่ยวนำให้อักเสบด้วย lipopolysaccharide (LPS) พบว่าสารสกัดไพลมีฤทธิ์ลดการเกิดการสะสมของreactive oxygen species ในเซลล์ที่ทดสอบได้ (24)
การวิเคราะห์แยกสาร cassumunarins A, B และ C จากเหง้าไพล ใช้สารสกัดอะซีโตน 111 ก. (สกัดจากเหง้าไพลสด 2.9 กก.) แยกวิเคราะห์สารด้วย silica gel chromatography ทดสอบฤทธิ์ต้านอนุมูลอิสระโดยการวัดautooxidationของกรดไขมันlinoleicในระบบ buffer-ethanol system พบว่ามีฤทธิ์ในการยับยั้งการสะสมของ lipid hydroperoxide ได้ (18)
การทดสอบฤทธิ์ต้านอนุมูลอิสระของสาร cassumunin A และcassumunin B ที่แยกได้จากไพล ต่อเซลล์ thymocyteของหนู ในหลอดลดลอง พบว่าสาร cassumuninsขนาด 10 นาโนโมล - 3 ไมโครโมล มีฤทธิ์ป้องกัน hydrogen peroxide (H2O2) ที่ทำให้ลดการมีชีวิตรอดของเซลล์ (cell viability) ได้ (19)
ฤทธิ์ต้านอักเสบ (S014)
การศึกษาฤทธิ์ต้านการอักเสบของผงไพลแห้งจากกรุงเทพมหานคร สกัดด้วยเทคนิค supercritical CO2 fluid ได้สารสกัดที่มีองค์ประกอบหลัก คือ 1,4-bis(methoxy)triquinacene, terpinen-4-ol, 1,4,7-tris(methoxy)triquinacene, α-terpinene, sabinene hydrate, และ DMPBD และเมื่อนำไปทดสอบฤทธิ์ต้านการอักเสบในเซลล์แมคโครฟาจ RAW 264.7 ที่ถูกเหนี่ยวนำให้อักเสบด้วย LPSพบว่าสารสกัดดังกล่าวมีฤทธิ์ในการยับยั้งค่าตัวชี้วัดการอักเสบ ได้แก่ nitric oxide, inducible nitric oxide synthase, cyclooxygenase-2, interleukin (IL)-1β, IL-6และ monocyte chemoattractant protein-1 ได้ (24)
การศึกษาฤทธิ์ต้านการอักเสบของสาร cassumunarins A, B และ C ที่แยกได้จากสารสกัดอะซีโตน ที่สกัดจากเหง้าไพลสด โดยทดสอบฤทธิ์ต้านการอักเสบในหนูเมาส์โดยทาสาร cassumunarins A, B และC 0.6 ไมโครโมลบริเวณหูทางซ้ายหลังจากนั้น 30 นาที เหนี่ยวนำให้เกิดการบวมด้วยการทา 12-O-tetradecanoylphorbol13-acetate (TPA) 2 มคก. บริเวณหูทั้งซ้ายและขวาในหนูแต่ละตัว ผลการทดสอบพบว่าสาร cassumunarins A, B และCมีฤทธิ์ยับยั้ง TPA ในการเหนี่ยวนำอาการบวมได้ โดยมีค่าร้อยละของการยับยั้งเท่ากับ 75, 62 และ 62 % ตามลำดับ (18)
การทดสอบฤทธิ์ต้านการอักเสบของสาร DMPBD จากเหง้าไพลในหนูแรทที่ถูกเหนี่ยวนำให้หูบวมด้วย ethyl phenylpropiolate (EPP), arachidonic acid และ TPA และหนูแรทที่ถูกเหนี่ยวนำให้อุ้งเท้าบวมด้วยการฉีดสารcarrageenan หรือplatelet-activating factor (PAF)ผลการทดสอบพบว่าการทาสาร DMPBD ในหนูที่ถูกเหนี่ยวนำให้บวมด้วย EPP มีฤทธิ์ยังยั้งอาการบวมด้วยค่า IC50 เท่ากับ 21 นาโนโมล ในขณะที่สาร oxyphenbutazone มีค่า IC50เท่ากับ 136 นาโนโมลและการทาสาร DMPBD ในหนูที่ถูกเหนี่ยวนำด้วย AA มีฤทธิ์ยังยั้งอาการบวมด้วยค่า IC50 เท่ากับ 60 นาโนโมลในขณะที่ยา phenidone มีค่า IC50 เท่ากับ 2520 นาโนโมล การทาสารDMPBD ในหนูที่ถูกเหนี่ยวนำด้วยTPA มีฤทธิ์ยังยั้งอาการบวมด้วยค่า IC50เท่ากับ 660 พิโคโมล ในขณะที่ยาdiclofenac มีค่า IC50 เท่ากับ 7200 พิโคโมล นอกจากนี้พบว่าสาร DMPBD และ diclofenac มีประสิทธิภาพใกล้เคียงกันในการยับยั้งการอักเสบของอุ้งเท้าหนูแรทที่เกิดจาก carrageenan แต่ไม่มีผลในหนูที่ถูกเหนี่ยวนำด้วย PAF (7)
การทดสอบฤทธิ์ต้านการอักเสบของสาร phenylbutenoids จากเหง้าไพล (Surabaya, Indonesia) ต่อการยับยั้งเอนไซม์ในกระบวนการอักเสบคือ cyclooxygenase-2 ในเซลล์แมคโครฟาจ RAW 264.7 ของหนูเมาส์ที่ถูกเหนี่ยวนำให้เกิดการอักเสบด้วย LPS ผลการทดสอบพบว่าสามารถแยกสารได้ 7 ชนิด สาร phenylbutenoid dimer 2 ชนิด มีฤทธิ์ในการยับยั้ง cyclooxygenase-2 โดยมีค่า IC50เท่ากับ 2.71 และ 3.64 ไมโครโมลาร์และสาร phenylbutenoid monomer 2 ชนิดมีฤทธิ์ในการยับยั้ง cyclooxygenase-2 มีค่า IC50เท่ากับ 14.97 และ 20.68 ไมโครโมลาร์ (9)
การศึกษาทางพิษวิทยาและความปลอดภัย
การทดสอบความเป็นพิษเฉียบพลันของสารสกัดเหง้าไพลด้วยเอทานอลในหนูแรทโดยให้สารสกัดทางปากขนาด 5,000 มก./กก.นน.ตัว ครั้งเดียวพบว่าไม่ก่อให้เกิดความเป็นพิษและการตายของหนูแรท และทดสอบพิษเรื้อรังโดยแบ่งหนูแรทออกเป็นกลุ่มทดสอบ 6 กลุ่ม ให้สารสกัดทางปาก ขนาด 0.3, 3, 30, 11.25, 112.5 และ 1,125 มก./กก.นน.ตัว/วัน ตามลำดับ เป็นระยะเวลา 270 วัน และกลุ่มควบคุมให้ยาหลอกพบว่าไม่ก่อให้เกิดความเป็นพิษและไม่พบอาการไม่พึงประสงค์ใด ๆ (25)
การศึกษาพิษเฉียบพลันของสารสกัดไพลด้วยแอลกอฮอล์และสารสกัดไพลด้วยเฮกเซน โดยให้สารสกัดทางปาก พบว่าสารสกัดทั้งสองมีขนาดที่ทำให้หนูตายร้อยละ 50 (LD50) เท่ากับ 20 และ 80 ก./กก. ตามลำดับ (ขนาดที่ใช้รักษาในคนเท่ากับ 10-20 มก./กก.) ส่วนการศึกษาพิษเรื้อรัง โดยให้หนูกินอาหารผสมกับไพลขนาดร้อยละ 0.5, 3 และ 18 ของน้ำหนักอาหาร (เท่ากับ 23, 150 และ 1,200 เท่าของขนาดที่ใช้รักษาในคน ตามลำดับ) พบว่าไพลขนาดร้อยละ 18 ของน้ำหนักอาหาร ส่งผลให้หนูมีน้ำหนักลดลง เมื่อตรวจปัสสาวะ ค่าชีวเคมีในเลือด และลักษณะทางพยาธิวิทยา ไม่พบความผิดปกติใดๆ (26)
ข้อห้ามใช้
- ห้ามทาบริเวณขอบตาและเนื้อเยื่ออ่อน
- ห้ามทาบริเวณผิวหนังที่มีบาดแผลหรือมีแผลเปิด
ข้อควรระวัง
ยังไม่มีรายงานข้อควรระวังในรูปแบบเครื่องสำอาง
อาการไม่พึงประสงค์
ยังไม่มีรายงานอาการไม่พึงประสงค์ในรูปแบบเครื่องสำอาง
ขนาดที่แนะนำ (ข้อมูลจากการศึกษาทางคลินิก)
ผลิตภัณฑ์เกี่ยวกับผิวหน้า
เจลที่ทําจากน้ำมันไพลปริมาณ 1% ใช้วันละ 2 ครั้ง ตอนเช้าและเย็นหลังล้างหน้าหลังจากเช็ดหน้าให้แห้งจึงแต้มสิวโดยทารอบ ๆ บริเวณที่เป็นสิวและบริเวณที่มักจะเป็นสิวชนิดเล็กน้อยถึงปานกลาง (6)
สิทธิบัตร
DIP (THAILAND-TH)
สรุป
ไพลเป็นสมุนไพรไทยชนิดหนึ่งที่มีการใช้ประโยชน์อย่างแพร่หลาย มีการใช้น้ำมันไพลเพื่อบรรเทาอาการปวดและอักเสบ และมีงานวิจัยของไพลที่มีฤทธิ์ทางเภสัชวิทยาที่อาจเป็นข้อมูลในการใช้ประโยชน์เกี่ยวกับเครื่องสำอาง มีการศึกษาทางคลินิกการใช้น้ำมันหอมระเหยจากไพลเป็นส่วนผสมในผลิตภัณฑ์เจลแต้มสิว และการทดสอบฤทธิ์ในการต้านแบคทีเรียสาเหตุของการเกิดสิว ฤทธิ์ต้านอนุมูลอิสระ และฤทธิ์ต้านการอักเสบ
เอกสารอ้างอิง
1. ราชันย์ ภู่มา, สมราน สุดดี, บรรณาธิการ. ชื่อพรรณไม้แห่งประเทศไทยเต็มสมิตินันท์ฉบับแก้ไขเพิ่มเติมพ.ศ. 2557. กรุงเทพฯ: สำนักงานหอพรรณไม้สำนักวิจัยการอนุรักษ์ป่าไม้และพันธุ์พืชกรมอุทยานแห่งชาติสัตว์ป่าและพันธุ์พืช; 2557.
2. Zingibermontanum (J.Koenig) Link ex A.Dietr. The World Flora Online. [Internet]. [cited 2021 Nov 11]. Available from:http://www.worldfloraonline.org/taxon/wfo-0000617206
3. นันทวัน บุณยะประภัศร, อรนุช โชคชัยเจริญพร, บรรณาธิการ. สมุนไพร..ไม้พื้นบ้าน (3). กรุงเทพฯ: บริษัทประชาชนจำกัด; 2542.
4. De Guzman CC, Siemonsma JS. Prosea: Plant Resources of South-East Asia No 13 Spices. Leiden: Backhuys Publishers, 1999:400 pp.
5. สุธรรม อารีกุล, จำรัส อินทร, สุวรรณ ทาเขียว, อ่องเต็ง นันทแก้ว. องค์ความรู้เรื่องพืชป่าที่ใช้ประโยชน์ทางภาคเหนือของประเทศไทยเล่ม3. กรุงเทพฯ: มูลนิธิโครงการหลวงบริษัทอมรินทร์พริ้นติ้งแอนด์พับลิชชิ่งจำกัด (มหาชน), 2551:886หน้า.
6. จุฬาภรณ์ ลิมวัฒนานนท์, ธนนรรจ์ รัตนโชติพานิช, อารีวรรณ เชี่ยวชาญวัฒนา และคณะ. ประสิทธิผลทางคลินิกของเจลไพลที่ทำจากน้ำมันไพลปริมาณ 1% ในการรักษาสิวชนิดเล็กน้อยถึงปานกลาง. วารสารเภสัชศาสตร์อีสาน. 2551;4(2):121-33.
7. Jeenapongsa R, Yoovathaworn K, Sriwatanakul KM, Pongprayoon U, Sriwatanakul K. Anti-inflammatory activity of (E)-1-(3,4-dimethoxyphenyl) butadiene from ZingibercassumunarRoxb. J Ethnopharmacol. 2003;87(2-3):143-8. doi: 10.1016/s0378-8741(03)00098-9.
8. Cb Singh, Manglembi N, Swapana N, Sb Chanu. Ethnobotany, phytochemistry and pharmacology of ZingibercassumunarRoxb. (Zingiberaceae). J PharmacognPhytochem. 2015;4(1):1-6.
9. Han AR, Kim MS, Jeong YH, Lee SK, Seo EK. Cyclooxygenase-2 inhibitory phenylbutenoids from the rhizomes of Zingibercassumunar. Chem Pharm Bull (Tokyo). 2005;53(11):1466-8. doi: 10.1248/cpb.53.1466. PMID: 16272734.
10. Nakamura S, Iwami J, Matsuda H, Wakayama H, Pongpiriyadacha Y, Yoshikawa M. Structures of new phenylbutanoids and nitric oxide production inhibitors from the rhizomes of Zingibercassumunar. Chem Pharm Bull (Tokyo). 2009;57(11):1267-72. doi: 10.1248/cpb.57.1267.
11. Sukatta U, Rugthaworn P, Punjee P, Chidchenchey S, Keeratinijakal V. Chemical composition and physical properties of oil from Plai (ZingibercassumunarRoxb.) obtained by hydro distillation and hexane extraction. Kasetsart Journal (Natural Science) (Thailand). 2009;43(5):212-7.
12. Devkota HP, Paudel KR, Hassan MM, Dirar AI, Das N, Devkota AA, et al. Bioactive compounds from Zingibermontanum and their pharmacological activities with focus on zerumbone. Appl Sci. 2021;11:10205. doi: 10.3390/app112110205.
13. Han AR, Kim H, Piao D, Jung CH, Seo EK. Phytochemicals and bioactivities of ZingibercassumunarRoxb. Molecules. 2021;26(8):2377. doi:10.3390/molecules26082377.
14. Khemawoot P, Hunsakunachai N, Anukunwithaya T, Bangphumi K, Ongpipattanakul B, Jiratchariyakul W, et al. Pharmacokinetics of compound D, the major bioactive component of Zingibercassumunar, in rats. Planta Med. 2016;82(13):1186-91. doi: 10.1055/s-0042-104658.
15. อาพาภรณ์ แก้วชูทอง. การเตรียมและการควบคุมคุณภาพสารสกัดไพลที่มีสารออกฤทธิ์ต้านการอักเสบปริมาณสูง [วิทยานิพนธ์ปริญญาวิทยาศาสตรมหาบัณฑิต]. สงขลา: มหาวิทยาลัยสงขลานครินทร์; 2552.
16. Verma RS, Joshi N, Padalia RC, Singh VR, Goswami P, Verma SK, et al. Chemical composition and antibacterial, antifungal, allelopathic and acetylcholinesterase inhibitory activities of cassumunar-ginger. J Sci Food Agric. 2018;98(1):321-327. doi: 10.1002/jsfa.8474.
17. Kabkrathok P, Jarussophon S, Unger O, Lomarat P, Reutrakul V, Pittayanurak P, et al. Mass spectral analysis of secondary metabolites from Zingibermontanum rhizome extract using UHPLC-HR-ESI-QTOF-MS/MS. Phytochem Anal. 2021. doi: 10.1002/pca.3068.
18. Masuda T, Jitoe A, Mabry TJ. Isolation and structure determination of cassumunarins A, B, and C: New anti-inflammatory antioxidants from a tropical ginger,Zingibercassumunar. J Am Oil Chem Soc. 1995;72(9):1053-7. doi: 10.1007/BF02660721.
19. Nagano T, Oyama Y, Kajita N, Chikahisa L, Nakata M, Okazaki E, et al. New curcuminoids isolated from Zingibercassumunar protect cells suffering from oxidative stress: a flow-cytometric study using rat thymocytes and H2O2. Jpn J Pharmacol. 1997;75(4):363-70. doi: 10.1254/jjp.75.363.
20. Department of Medical Sciences, Ministry of Public Health. Thai Herbal Pharmacopeia Volume II. Bangkok: The Agricultural Co-operative Federation of Thailand., Ltd. 2020.
21. Saeio K, Chaiyana W, Okonogi S. Antityrosinase and antioxidant activities of essential oils of edible Thai plants. Drug DiscovTher. 2011;5(3):144-9. doi: 10.5582/ddt.2011.v5.3.144.
22. Luangnarumitchai S, Lamlertthon S, Tiyaboonchai W. Antimicrobial activity of essential oils against five strains of Propionibacterium acnes. MahidolUniv J Pharm Sci. 2007;34(1-4):60-4.
23. Pithayanukul P, Tubprasert J, Wuthi-Udomlert M. In vitro antimicrobial activity of Zingibercassumunar (Plai) oil and a 5% Plai oil gel. Phytother Res. 2007;21(2):164-9. doi: 10.1002/ptr.2048.
24. Truong VL, Manochai B, Pham TT, Jeong WS. Antioxidant and anti-Inflammatory activities of Zingibermontanumoil in HepG2 cells and lipopolysaccharide-stimulated RAW 264.7 macrophages. J Med Food. 2021;24(6):595-605. doi: 10.1089/jmf.2021.k.0019.
25. Koontongkaew S, Poachanukoon O, Sireeratawong S, Dechatiwongse Na Ayudhya T, Khonsung P, Jaijoy K, et al. Safety Evaluation of ZingibercassumunarRoxb. rhizome extract: acute and chronic toxicity studies in rats. IntSch Res Notices. 2014;2014:632608. doi: 10.1155/2014/632608.
26. Panyathanya R, Gnamwat W, Chawalidthumrong P, Permpipat U, Leelakulthanit O, Chantachaya C. Study of acute and chronic toxicity of Plai (ZingibercassumunarRoxb.) in rats. SirirajHosp Gaz. 1986;38:413-6.
27. ไพล. คู่มือการปลูกสมุนไพรสถาบันการแพทย์แผนไทยกรมการแพทย์แผนไทยและการแพทย์ทางเลือกกระทรวงสาธารณสุข[อินเทอร์เน็ต]. [เข้าถึงเมื่อ30กันยายน2564 ]. เข้าถึงจาก: https://ittm.dtam.moph.go.th/images/knowleaga/3/70%E0%B9%84%E0%B8%9E%E0%B8%A5%20%E0%B8%AB%E0%B8%99%E0%B9%89%E0%B8%B2186-188.pdf
P029_(18).xlsx